電解——作用原理、目的和應用
電解過程
 電解在有色金屬冶金和許多化學工業中很普遍。鋁、鋅、鎂等金屬主要通過電解獲得。此外,電解還用於提煉(提純)銅、鎳、鉛,以及生產氫氣、氧氣、氯氣和許多其他化學品。
電解在有色金屬冶金和許多化學工業中很普遍。鋁、鋅、鎂等金屬主要通過電解獲得。此外,電解還用於提煉(提純)銅、鎳、鉛,以及生產氫氣、氧氣、氯氣和許多其他化學品。
電解的本質是當直流電通過電解槽時,物質顆粒從電解液中分離出來,並沉積在浸入電解槽中的電極上(電萃取),或者當物質通過電解液從一個電極轉移到另一個電極時(電解精煉)。在這兩種情況下,過程的目標都是獲得未被雜質污染的最純淨的物質。
相比之下 電子電導率 電解質中的金屬(鹽、酸和鹼在水中和某些其他溶劑以及熔融化合物中的溶液),觀察到離子電導率。
電解質是第二類導體。在這些溶液和熔體中,會發生電解解離——帶正電和帶負電的離子分解。
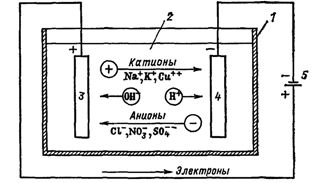
如果將連接到電源的電極放置在帶有電解質的容器中 - 電解槽,那麼離子電流將開始在其中流動,帶正電的離子 - 陽離子將移動到陰極(主要是金屬和氫),以及帶負電的離子——陰離子(氯、氧)——到陽極。
在陽極,陰離子失去電荷並變成中性粒子並沉積在電極上。在陰極,陽離子從電極獲取電子並被中和,沉澱在電極上,以氣泡形式釋放到電極上的氣體上升。
米。 1.電解過程。電浴電路:1—電槽,2—電解液,3—陽極,4—陰極,5—電源
外電路中的電流是電子從陽極到陰極的運動(圖 1)。在這種情況下,溶液被耗盡,為了保持電解過程的連續性,必須對其進行富集。這就是從電解質中提取某些物質的方式(電提取)。

如果將電極放置在含有相同物質離子的溶液中,則在電極和溶液之間的特定電勢下,電極既不會溶解,也不會從溶液中沉積物質。
這種電位稱為物質的正常電位。如果向電極施加更負的電勢,則會開始釋放物質(陰極過程),但如果施加更正的電勢,則會開始溶解(陽極過程)。
正常電位的值取決於離子濃度和溫度。人們普遍認為氫的正常電勢為零。表1顯示了一些物質水溶液在+25℃時的標準電極電位。
表 1. + 25 °C 時的正常電極電位
如果電解液中含有不同金屬的離子,則負法線電位較低的離子(銅、銀、鉛、鎳)首先在陰極分離;鹼土金屬是最難分離的。此外,水溶液中始終存在氫離子,比所有具有負法向電位的金屬更早釋放氫離子,因此後者在電解過程中,有相當一部分甚至大部分的能量都花在了氫離子的釋放上。 .
借助特殊措施,可以在一定限度內防止氫氣的產生,但不能通過電解獲得正常電位低於 1 V 的金屬(例如,鎂、鋁、鹼土金屬)水溶液。它們是通過分解這些金屬的熔鹽獲得的。
表中所示物質的正常電極電位。1, 在電解過程開始時是最小的,實際上,過程的發展需要大的電位值。
電解時電極的實際電位與其正常電位之間的差值稱為過電壓。它增加了電解過程中的能量損失。
另一方面,增加氫離子的過電壓使其難以在陰極釋放,這使得通過電解從水溶液中獲得許多比氫負性更強的金屬成為可能,例如鉛,錫,鎳、鈷、鉻甚至鋅。這是通過在電極上增加電流密度以及將某些物質引入電解質中來進行該過程來實現的。
電解過程中陰極和陽極反應的過程由以下兩個法拉第定律決定。
1. 電解時物質在陰極釋放或從陽極傳遞到電解液的質量md與通過電解液的電量Azτ成正比:me = α/τ,這裡a是該物質的電化學當量, GC。
2、等量電量電解時放出物質的質量與物質A的原子質量成正比,與其化合價n成反比:mNS = A / 96480n,這裡96480是法拉第數,C x mol -1。
這樣,一種物質的電化學當量α= A / 96480n 就代表單位電量通過電解槽所釋放的物質的質量,單位為克——庫侖(安培秒)。
對於銅 A = 63.54,n = 2,α =63.54/96480-2= 0.000329 g / C,對於鎳 α = 0.000304 g / C,對於鋅 α = 0.00034 g / C

物質實際釋放的質量與其根據法拉第定律應釋放的質量之比稱為該物質的電流產率η1。
因此,對於一個真實的過程 mNS = η1 NS (A / 96480n) NS 它
自然地,總是 η1
電流效率顯著取決於電極的電流密度。隨著電極電流密度的增加,電流效率增加,工藝效率增加。
提供給電解槽的電壓 Uel 包括:擊穿電壓 Ep(陽極和陰極反應的電位差)、陽極和陰極過電壓的總和、電解液中的電壓降 Ep、電解液中的電壓降 Ue = IRep(Rep — 電解電阻),輪胎、觸點、電極中的電壓降 Uc = I(Rw +Rto +RNS)。我們得到:Uel = Ep + Ep + Ue + Us。
電解時消耗的功率等於:Rel = IUmail = I(Ep + Ep + Ue + Uc)
在這種能量中,只有第一部分用於進行反應,其餘部分是該過程的熱損失。僅在熔融鹽的電解過程中,電解質 IUe 中釋放的部分熱量才得到有效利用,因為它用於熔化電解槽中裝入的鹽。
電解槽的效率可以通過每消耗 1 焦耳電能所釋放的物質質量(以克為單位)來估算。這個值稱為物質的能量產率,可以通過表達式qe = (αη1) /Uel100求出,這裡α——物質的電化學當量,g/C,η1——電流輸出,Uemail——電解電壓細胞,V.