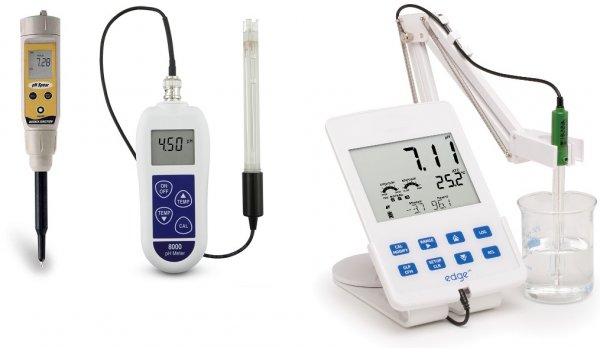
pH測量原理、裝置及pH計的種類
為了快速確定各種介質的 pH 值(換句話說,酸度值),需要使用 pH 計。工業或飲用水、酸、鹽或鹼溶液、血液、尿液和其他體液、水果、蔬菜和其他食品、醫療藥品等。 ——原則上,任何東西都可以成為運籌學pH值的對象。
測量 PH 值本質上是測量介質中氫離子的活性。甚至名稱 pH 本身也是從拉丁文“pondus Hydrogenii”直譯為“氫的重量”。
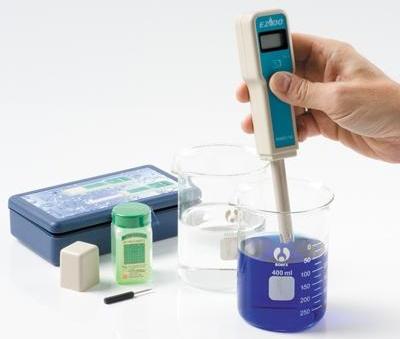
如今,pH 計廣泛應用於微生物學和醫學、水處理和農業化學、土壤科學、水培學、實驗室和實地研究、化學和食品工業、水族養殖以及許多其他領域。
現代 pH 計可讓您準確快速地確定 pH 值。如果pH為7,則介質呈中性,如蒸餾水,其中正氫離子H+和負氫氧根離子OH-均分。如果酸度大於 7,則介質呈鹼性。如果 pH 小於 7,則介質呈酸性。
儘管化學家總是能夠通過經典方法使用指示劑(例如酚酞)來確定介質的酸度,但是,在某些過程中,只需要準確地量化該指示劑,有時還需要不斷監測它,安排更正它。這就是發明 pH 計的目的。
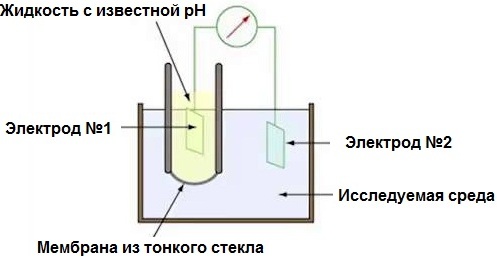
pH 計實際上是一個電子毫伏表,因為它測量一對電極的電化學系統和放置它們的測試介質之間的電位差。的確,設備的刻度在這裡不是以毫伏為單位,而是以 pH 為單位,因為測得的 EMF 與 pH 成正比。
兩個電極:一個玻璃指示劑(氧化劑不怕硼矽酸鹽玻璃)和氯化銀——一個附加的參比電極。玻璃電極的電阻非常高,幾十兆歐,這只是基本要求——探頭電阻不低於0.1 GΩ。使用已知 pH 值的緩衝溶液校準 pH 計。
由於 EMF 值受溫度影響,因此每個此類測量設備都具有溫度補償,可在 + 25°C 以外的溫度下進行測量。但是為了達到非常高的精度,需要在+25°C的溫度下進行精確測量,這就是為什麼很多pH計都配備了內置溫度計,這樣你就可以立即跟踪介質的溫度在研究的過程。
指示器玻璃電極呈管狀,末端有一個薄壁球,由特殊的導電硼矽酸鹽玻璃製成,基本上與電路相連。正 H + 離子在這種玻璃內部的移動使其成為可能(玻璃內部的陽離子相對於矽酸的聚陰離子移動)。將氯化銀在鹽酸溶液中的懸浮液倒入試管中,然後將銀線浸入其中 - 這就是獲得氯化銀電極的方法。
將玻璃電極降低到測試介質中,通過將額外的參考電極(氯化鉀溶液中的汞甘汞糊)放入其中(通過電解開關或直接)來閉合電路。氯化鉀在電池的汞-甘汞部分和測試介質之間產生接觸。這個附加電極通常放置在 H + 離子不能透過的玻璃外殼中。
參比電極中的氯化鉀溶液與試液的導電接觸是通過玻璃殼中的細線或毛細管形成的。這樣,由參比電極和氯化銀電極得到原電池,並且電池的電解質部分包括導電玻璃膜和測試環境。
電極系統的 EMF 用毫伏表測量,其刻度以 pH 計。來自氯化銀電極的電子在被測電動勢的作用下轉移到參比電極,這總是伴隨著等量的質子從玻璃電極內部轉移到介質中。
如果在這種情況下我們將正氫離子 H + 的濃度取為玻璃電極常數,則 EMF 將是 H + 活性的函數,即所研究介質 pH 值的函數。
現代型號的 pH 計的工作歸功於執行溫度補償並解決許多相關任務的微處理器。設備越複雜,它可以解決的任務就越多。儀器的精度等級因型號而異,可以針對不同的應用選擇合適的 pH 計。
有袖珍型家用pH計,有專業的實驗室用的、便攜式的和工業固定式的。一些pH計測量介質中的離子濃度、硝酸鹽含量等,具有內置存儲器存儲結果,具有與計算機通訊的能力和通過反饋迴路調整參數的功能。