石墨烯和石墨有什麼區別?
碳是一種非凡的化學元素,位於化學元素週期表第二週期第十四族中的第 6 位。自古以來,人們就知道金剛石和石墨,這是迄今為止發現的該元素九種以上的同素異形變體中的兩種。順便說一句,與其他物質相比,現代科學已知的同素異形體修飾數量最多的是碳。
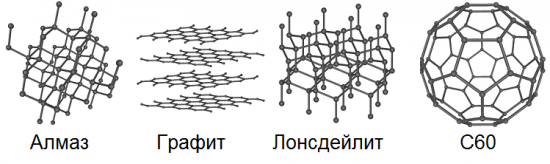
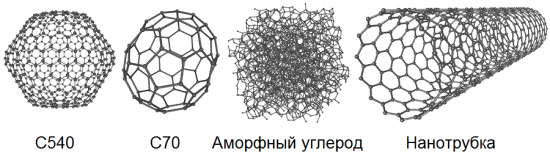
同素異形體是指同一化學元素在自然界中可能以兩種或兩種以上的單質形式存在,即所謂的同素異形體或同素異形體變體,從而導致這些物質在結構和性質上存在差異。所以,碳有8種這樣的基本形式:金剛石、石墨、方石、富勒烯(C60、C540和C70)、無定形碳和單壁納米管。
在這些形式的碳中,有完全不同的性質和特性:軟的和硬的、透明的和不透明的、便宜的和昂貴的物質。然而,讓我們比較一下兩種相似的碳變體——石墨和石墨烯。

我們從學校開始就熟悉塗鴉。普通鉛筆的鉛芯就是石墨。它摸起來非常柔軟、光滑和油膩,晶體是板狀的,原子層一層一層地放置,因此當摩擦時,例如在紙上,石墨層狀晶體結構的單個薄片很容易剝落, 在紙上留下特徵性的黑色痕跡。
石墨導電性好,其電阻平均為11 Ohm * mm2 / m,但由於其晶體的天然各向異性,石墨的電導率並不相同。因此,沿晶體平面的電導率比這些平面的電導率高數百倍。石墨的密度為2.08至2.23克/立方厘米。
在自然界中,石墨是在高溫下在火成岩和火山岩、矽卡岩和偉晶岩中形成的。它發生在石英脈和熱液中溫多金屬礦床中的礦物中。廣泛分佈於變質岩中。
因此,自1907年以來,世界上最大的天然鱗片石墨儲量就在馬達加斯加島上開發出來。該島由前寒武紀變質岩組成,這些岩石在山區地形中升至地表,測高標記為 4,000-4,600 英尺。石墨產於 400 英里長的帶中,在該島中心東部的山脈中占主導地位。
與石墨不同,石墨烯沒有塊狀晶體結構;它具有二維六方晶格,只有一個原子厚。在這種同素異形體修飾中,碳根本不會自然產生,但理論上可以通過人工獲得。我們可以說,故意從石墨的多層塊狀晶體結構中分離出來的平面就是這種石墨烯。
由於這種形式的物質不穩定,科學家們最初無法獲得簡單二維薄膜形式的石墨烯。然而,在氧化矽襯底上(由於與介電層的鍵合)仍然有可能獲得一個原子厚的石墨烯:2004 年,俄羅斯科學家安德烈·蓋姆和曼徹斯特大學的康斯坦丁·諾沃肖洛夫在《科學》雜誌上發表了一篇報告以這種方式獲得石墨烯。
即使在今天,這種獲得石墨烯用於研究的簡單方法,例如使用膠帶(和類似方法)從大塊石墨晶體中機械剝離碳單層,也是合理的。
研究人員相信,由於他們的進步,很快就會出現一類新的基於石墨烯的納米電子學,其中場效應晶體管的厚度將小於 10 納米。事實上,石墨烯中的電子遷移率非常高 (10,000 cm2 / V * s),它似乎是當今最有希望替代傳統矽的材料。
高載流子遷移率是電子和空穴對施加電場的影響做出極快響應的能力,這對於場效應晶體管(現代電子產品的基本操作單元)極為重要。
在製造各種生物和化學傳感器以及用於光伏設備和触摸屏的薄膜方面也有前景。儘管如此,石墨烯的熱導率仍比銅高 10 倍,而這一標準對於電子產品始終非常重要。